Current Biology丨深圳先进院陈祖昕和刘欣安团队合作揭示压力应激正向强化作用的神经机制
by 管理员 | 2024-01-15
北京时间2024年1月12日,中国科学院深圳先进技术研究院脑认知和脑疾病研究所/深港脑科学创新研究院陈祖昕和刘欣安团队联合在Current Biology 杂志上发表题为 “Hypothalamic CRF neurons facilitate brain reward function” 的研究论文。研究团队发现了负责压力应激响应的下丘脑CRF神经元(PVNCRF)具有促进奖赏行为的作用,进一步揭示了PVNCRF-VTA-NAc是介导其中的关键神经环路,而并不依赖于经典的神经内分泌HPA轴。这项工作揭示了介导压力应激正向强化作用的神经基础,解释了人们喜欢紧张刺激活动(如坐过山车、观看体育比赛等)的背后机制。此外,该研究为治疗成瘾、焦虑、抑郁等与压力应激相关的精神疾病提供了潜在的靶点。

文章上线截图
点击文末“文章链接”查看全文
目前大多观点认为压力应激是促进焦虑、抑郁以及药物成瘾等精神疾病的重要因素。但是,在某些情况下,人们也会主动寻求压力刺激,比如喜欢坐过山车,高空跳伞,攀岩,观看竞技性体育比赛等引起紧张刺激感的活动或运动。这种行为在啮齿类动物中也是存在的,例如某些大鼠更喜欢去探索具有潜在威胁或引发压力应激的新环境。此外,压力应激会引起奖赏中枢多巴胺的分泌,这与大多数成瘾性物质一样。这些证据表明,压力应激也具有正向强化作用,具有奖赏性,而并不总是导致厌恶或者逃避等负性效应。然而,介导压力应激正向强化效应的神经基础以及机制尚未清楚。
位于下丘脑室旁核的CRF神经元(PVNCRF),是众所周知的介导和整合压力应激效应的重要脑区,在物种上具有保守性。这群神经元能被各种不同形式、不同强度的压力应激所激活,通过启动神经内分泌下丘脑-垂体-肾上腺(HPA)轴释放糖皮质激素来调动全身系统应对外界压力刺激。此外,它们还能实时双向编码压力刺激的效价,并调节动物的即时行为反应。人为反复激活这群神经元会导致条件性厌恶,因此,它们被认为在介导压力应激的负性效应中起到重要的作用。然而,这群神经元的激活并不总是产生负面效果,研究发现适度的压力应激通过激活这群神经元使得小鼠更容易适应环境。此外,HPA轴的终产物糖皮质激素本身具有正向强化效应。这些研究结果暗示,PVNCRF神经元的激活也可能在压力应激的正向强化中起作用,但尚未有直接证据。本研究工作针对以上科学问题进行了深入探讨。
首先,研究团队通过结合光遗传学工具(ChR2)和CRF-Cre转基因小鼠特定激活PVNCRF神经元,发现能显著促进self-grooming行为和升高血液糖皮质激素水平,这与此前众多文献报道一致。接下来,通过实时位置性偏好/厌恶实验范式(RTPP/A),发现激活这群神经元后,整体上并不产生显著性效果,但是仔细分析发现部分小鼠表现出明显的厌恶现象,而部分小鼠则表现出明显的偏好。进一步通过操控箱中的自我光刺激实验范式,发现所有ChR2小鼠都表现出明显的自我刺激行为(均值为300次/30分钟),而对照组小鼠则没有,表明PVNCRF神经元的激活具有典型的正向强化作用。
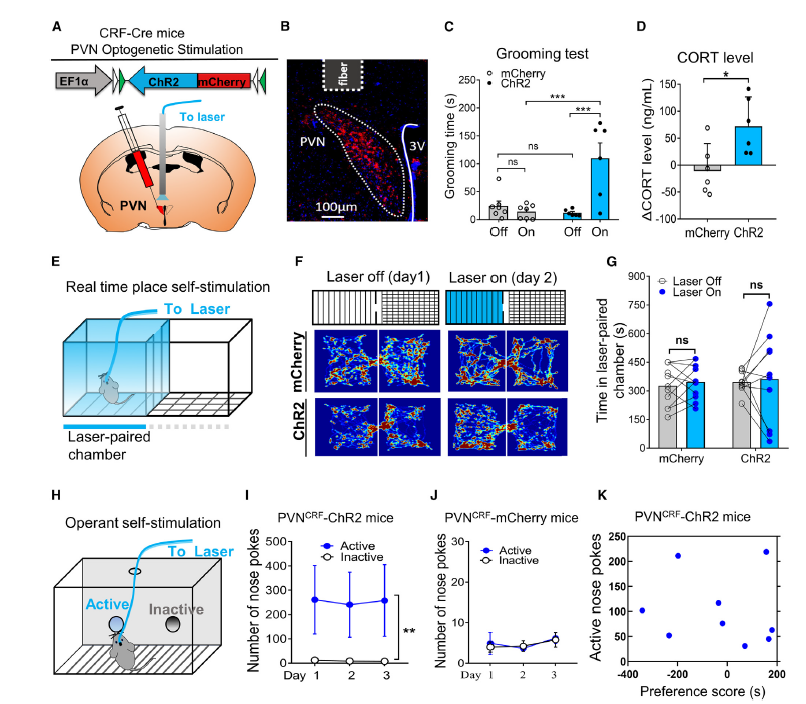
图1. PVNCRF神经元的激活具有正向强化作用
接着,研究团队通过量化小鼠在操控箱中的自我刺激次数,结合药理学手段,对PVNCRF神经元的奖赏效应进行了初步的机制分析。首先,药理学阻断HPA轴的激活及糖皮质激素受体拮抗剂并不能显著改变自我刺激次数,说明并不是由HPA轴所介导。腹腔注射CRF受体1,多巴胺D1受体拮抗剂均能显著降低自我刺激次数,而多巴胺D2受体,催产素受体拮抗剂均并不影响自我刺激次数。这些数据表明,PVNCRF神经元的奖赏效应可能依赖于经典的多巴胺奖赏环路。

图2. PVNCRF神经元的正向强化作用依赖于
CRF受体1和多巴胺D1受体
的确,研究团队在中脑腹侧被盖区(VTA)发现了大量的PVNCRF神经末梢。光遗传学激活这些神经末梢能引起小鼠显著的位置性偏好,和在操控箱中的强烈的自我刺激行为(均值为900次/30分钟),并且同样依赖于CRF受体1和多巴胺D1受体,而不影响self-grooming行为和血液糖皮质激素水平。这说明,PVNCRF→VTA神经环路是介导PVNCRF神经元奖赏效应的主要神经基础。
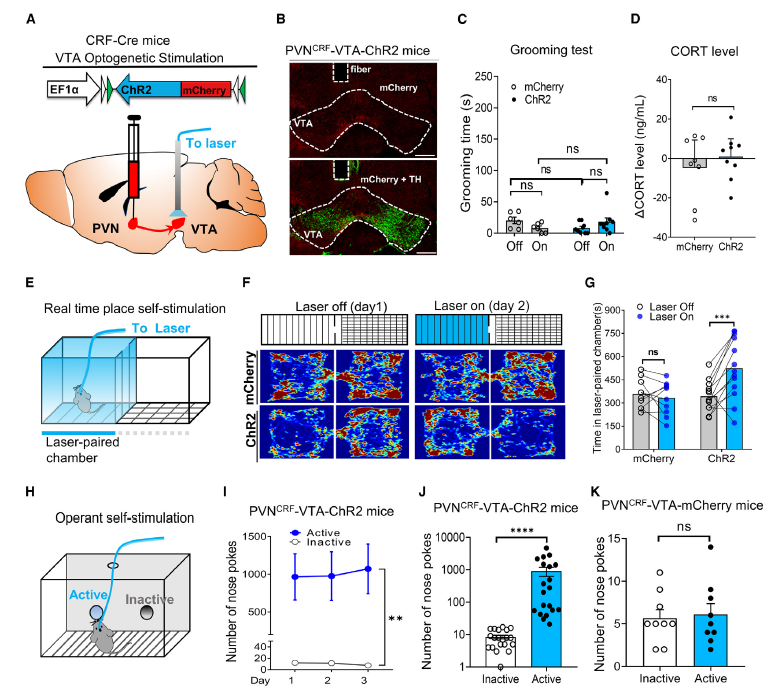
图3. 激活PVNCRF→VTA神经环路引起强烈的自我刺激行为

图4. PVNCRF→VTA的正向强化作用也依赖于
CRF受体1和多巴胺D1受体
为了阐明PVNCRF→VTA神经环路如何起作用,研究团队通过c-fos免疫荧光染色确定了这条环路的自我刺激增加多巴胺神经元活动。进一步通过结合多巴胺荧光探针和在体光纤光度记录技术,发现激活PVNCRF→VTA神经环路迅速引起多巴胺在伏隔核的释放。并且,在伏隔核定位注射多巴胺D1和D2受体拮抗剂均显著降低相应的自我光刺激次数。至此,研究团队鉴定出了PVNCRF→VTA→NAc神经环路是介导PVNCRF奖赏效应的重要神经基础。

图5. 激活PVNCRF→VTA神经环路促进多巴胺在伏隔核的释放

图6. PVNCRF→VTA→NAc是介导压力应激
正向强化作用的重要神经基础
总结,本研究首次揭示了PVNCRF神经元具有正向强化作用,并且首次对PVNCRF→VTA→NAc神经环路做了功能解析。鉴于大多数抑郁、药物成瘾患者对陌生环境表现出厌恶/回避性反应,说明压力应激的正向强化作用在这些患者中是受损的。并且,这些情绪障碍大多与多巴胺和CRF系统异常相关。因此,本研究揭示的神经机制将能促进对此类疾病发生发展的理解,为治疗相关疾病提供新的靶点和策略。
深圳先进院脑所陈祖昕和刘欣安副研究员为该论文的共同通讯作者,深圳先进院脑所博士后许新丽(已出站)、深圳先进院与广州医科大学联合培养硕士研究生郑水调(已毕业)、深圳先进院脑所博士后任嘉彦和中国科学院大学在读硕士研究生李子萱,为共同第一作者。研究论文的共同作者还包括深圳先进院脑所王立平、朱英杰、周涛等研究员及团队成员,广州医科大学附属中医院陈楚云副主任医师,北京大学深圳研究生院李书鹏教授及团队成员,和广州南方学院夏建勋副教授等。论文得到了1991年诺奖得主Erwin Neher教授、深圳理工大学(筹)韩明虎教授和UBC Anthony Phillips教授等人的宝贵建议和帮助。该论文还致谢了中国科学技术大学周江宁教授、刘际教授,以及徐州医科大学张红星教授为课题的开展提供了宝贵的实验材料。

部分团队合影,陈祖昕(共同通讯作者,左一),刘欣安(共同通讯作者,左四),任嘉彦(共同第一作者,左二),李子萱(共同第一作者,左三),徐智彬(共同作者,右二),夏建勋(共同作者,右一),杨其兴(共同作者,右四)
本研究致谢了科技部科技创新2030 “脑科学与类脑研究”重大项目、国家自然科学基金委员会、广东省基础与应用基础研究基金委员会、中国科学院脑联结解析与调控重点实验室、广东省脑连接图谱重点实验室、深圳市科创委、深港脑科学创新研究院、广州市科技计划项目等的资助与支持。

