Advanced Functional Materials丨深圳先进院脑所/深港脑院鲁艺团队研发激光诱导石墨烯生物电子器件并实现柔性多模态闭环脑机接口
神经系统疾病往往伴随神经环路功能紊乱与外周生理异常(如心率、呼吸节律改变)。同步监测电生理信号与生理信号,对于解析脑工作机制、实现精准诊疗至关重要。然而,现有生物电子器件在电化学性能与力学特性上的局限,使得跨物种建立电生理与生理信号动态变化的直接因果联系仍面临挑战,制约了柔性多模态脑机接口技术的发展,也限制了对"脑-体"相互作用的系统理解。激光诱导石墨烯(Laser-Induced Graphene, LIG)因制备便捷、图案化灵活且本征柔性,被视为构建可穿戴传感器与脑机接口的理想材料。但如何优化其微结构并设计功能界面,使其同时满足高灵敏生理传感(高拉伸性、高机电响应)与长期稳定神经记录(低阻抗、高电容、生物相容性)的双重需求,仍是亟待突破的应用瓶颈。
近日,中国科学院深圳先进技术研究院脑认知与脑疾病研究所/深港脑科学创新研究院/脑认知与类脑智能全国重点实验室鲁艺研究员团队在《Advanced Functional Materials》发表题为"Laser-Induced Graphene Bioelectronics for Flexible Multimodal Physiological-Electrophysiological Monitoring"的研究论文。该团队开发了一种基于LIG的多模态柔性脑机接口技术,可在人类、非人灵长类和啮齿类动物中实时同步监测生理信号(心率、呼吸等)与神经电生理信号,并在癫痫小鼠模型中实现了按需闭环调控干预。

文章上线截图,点击文末链接查看
研究团队通过优化激光加工参数与多步界面工程策略,制备了两种功能互补的LIG生物电子器件(如图1所示):
(1)双侧激光诱导石墨烯(BiL-LIG)传感器:具备高拉伸性与优异机电灵敏度,适用于可穿戴生理监测,可精准捕捉心跳、呼吸及肢体运动等生理信号。
(2)界面工程化激光诱导石墨烯(IntE-LIG)电极:通过沉积导电聚合物-金复合涂层,实现超低界面阻抗(1 kHz下阻抗降低98.5%)与高电荷存储能力,可制备为柔性神经电极阵列,用于长期稳定的在体神经活动记录。
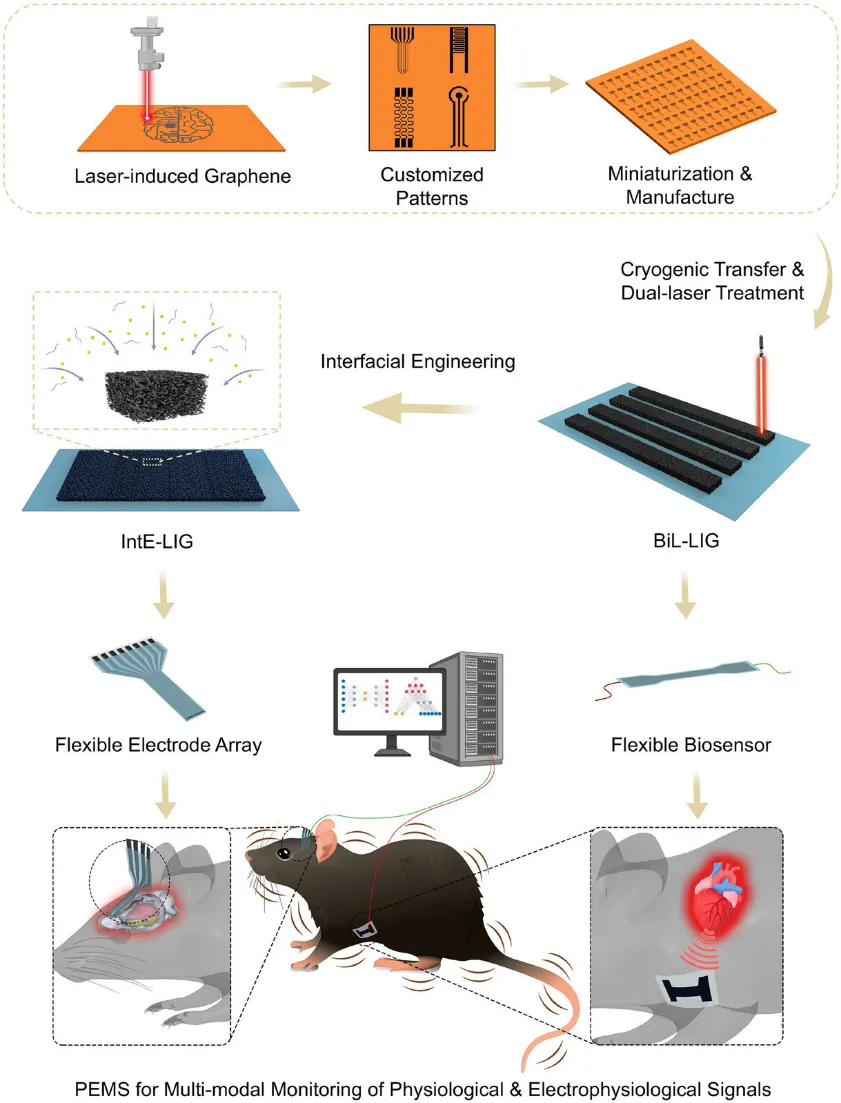
图1. 生理-电生理监测系统(PEMS)的制作过程示意图(来源:Advanced Functional Materials)
上述器件的跨物种适应性得到了充分验证(如图2、图3所示)。在人体志愿者上,LIG生物电子器件可清晰记录桡动脉脉搏波,精准捕捉从静息到高强度运动过程中心率与呼吸频率的动态变化。在非人灵长类实验动物(猕猴)上,BiL-LIG传感器成功监测到麻醉状态下的心率与呼吸频率,IntE-LIG电极则实现了至少4周的稳定电生理记录。在啮齿类实验动物(小鼠)上,超薄柔性BiL-LIG传感器以非侵入方式贴合胸腹部,测得的心率与呼吸频率均处于正常生理范围,IntE-LIG电极更实现了长达12周的稳定电生理记录。上述结果证明,LIG生物电子器件可满足跨物种动物模型对信号质量及器件-生物界面匹配性的严苛要求。
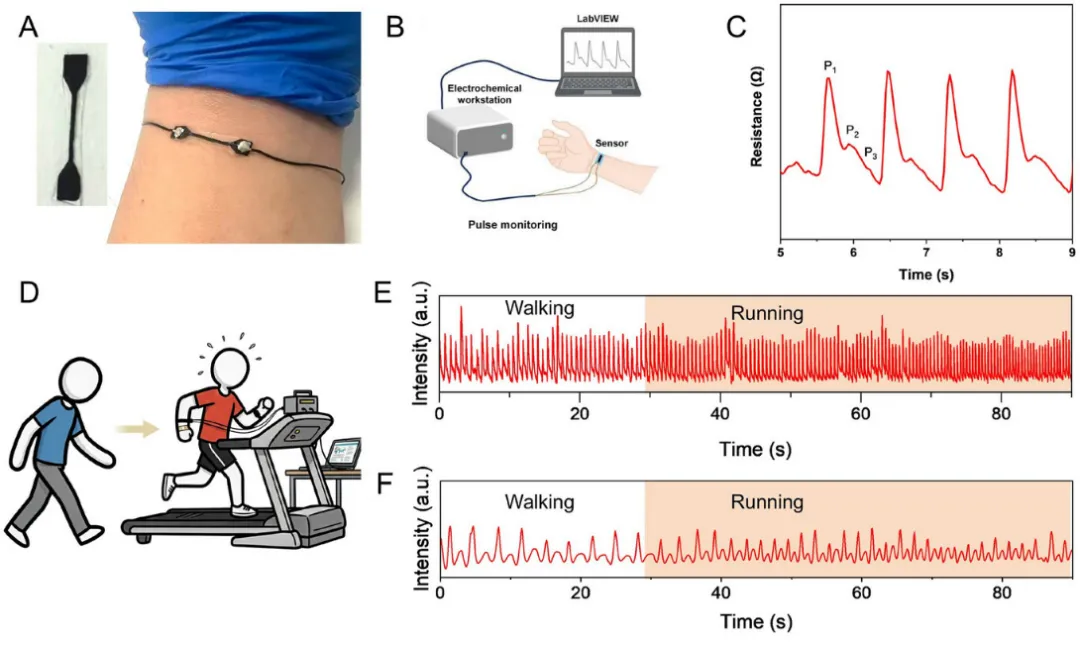
图2. LIG生物电子器件在人体上的生理信号监测(来源:Advanced Functional Materials)
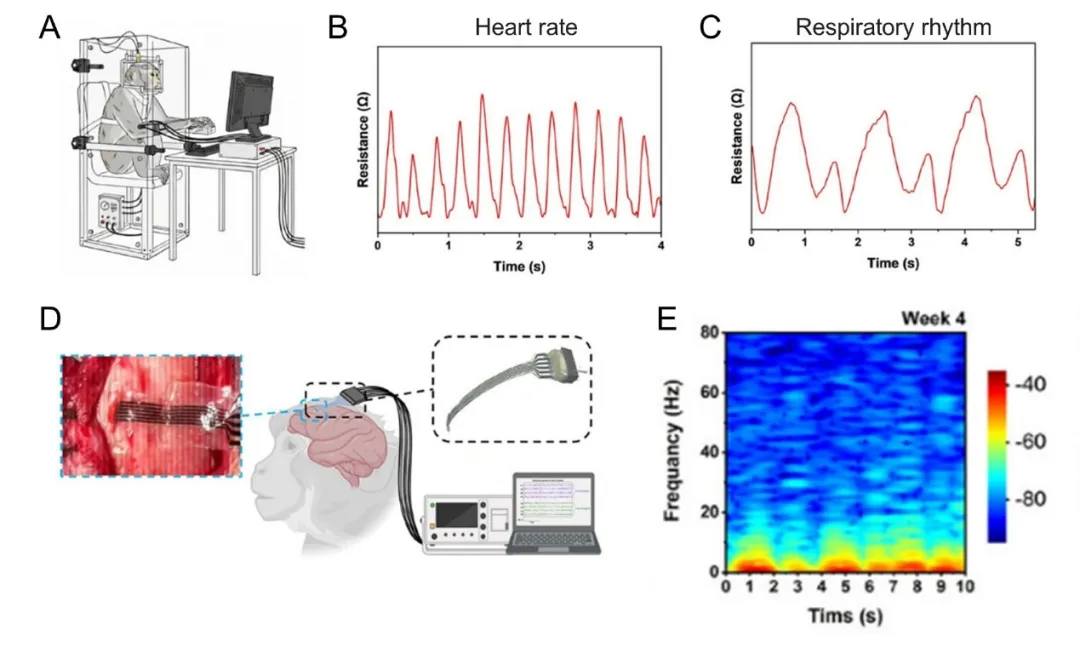
图3. BiL-LIG 和IntE-LIG在非人灵长类实验动物(猕猴)上分别进行生理信号监测和长期电生理记录(来源:Advanced Functional Materials)
基于上述互补器件,团队集成了柔性生理-电生理监测系统(PEMS),并在急性癫痫小鼠模型中完成概念验证(如图4所示)。正常状态下,PEMS同步记录皮层局部场电位(LFP)与心率基线;诱发急性癫痫发作后,系统同时捕捉到典型的癫痫放电波形增强与心率急剧升高的双重特征。一旦双模态信号超过设定阈值,系统自动触发微量注射泵给予抗癫痫药物拉莫三嗪。干预后,小鼠神经活动与心率均恢复至基线水平,展现了"监测-决策-干预"的闭环调控潜力。
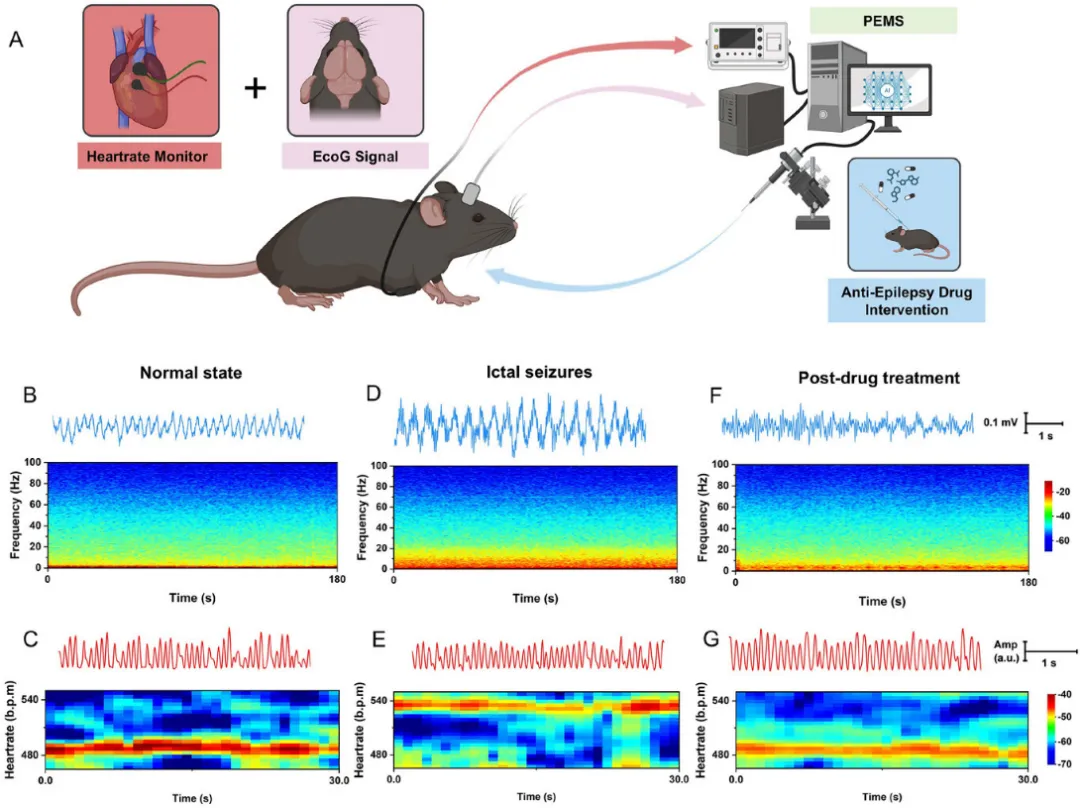
图4. 多模态生理-电生理监测系统(PEMS)的建立及其在癫痫检测与治疗中的应用(来源:Advanced Functional Materials)
该研究通过材料工程创新,统一了生理信号与神经电信号的在体监测技术路径,构建了一个可扩展、跨物种的多模态脑机接口平台。这不仅为癫痫的精准检测与即时干预提供了新型一体化工具,也为研究神经环路动态与机体生理状态的交互关系、推动神经精神疾病闭环调控疗法的发展奠定了技术基础。深圳先进院脑认知与脑疾病研究所鲁艺研究员为本文通讯作者,助理研究员廖鑫、博士后陆登宇、南京大学-深圳先进院联培博士生巫祎咏、中国科学技术大学联培硕士生陈亚鑫(已毕业)为共同第一作者。
近年来,鲁艺团队聚焦柔性脑机接口技术研发及其在病理神经环路干预中的应用,通过与多个团队合作,在植入式神经电极阵列及功能化神经界面领域取得系列进展(Advanced Materials 2023, 2025a&b; Advanced Functional Materials 2023, 2026; Advanced Healthcare Materials 2024; ACS Nano 2024),并对病理状态神经环路功能进行了深入解析(Cell Reports 2022; Nature Communications 2016)。本研究得到了国家科技创新-2030重大项目(青年科学家)、国家自然科学基金委(优青、面上项目)及广东省、深圳市各级项目资助。深圳市脑解析与脑模拟重大科技基础设施(脑设施)依托微纳平台、跨物种实验动物资源及跨尺度神经解析技术矩阵构建的"脑机接口生态体系",为本研究提供了全面支持。
论文链接:
https://doi.org/10.1002/adfm.202531604
